Рассеянный склероз
Первое описание болезни было составлено неврологом Жаном Мартеном Ширко (Франция) в 1868 году. Рассеянный энцефаломиелит (а именно таково научное название этого недуга) — аутоиммунное прогрессирующее хроническое заболевание нервной системы, протекание которого сопровождается постепенным поражением миелиновой оболочки нервных волокон головного и спинного мозга. Волокна соединяют центры мозга посредством электрических импульсов, ускорение скорости которых и обеспечивает миелин — электролизующее белое вещество липидно-белкового происхождения. Помимо этой функции оболочка выполняет и другую, не менее важную, — миелин изолирует нервные отростки друг от друга.
Причины появления и развития рассеянного склероза
Основным источником развития патологии являются многочисленные вирусы — это краснуха, паротит, герпес, корь, бешенство и ряд других. Проникая в нервные клетки, они живут в них годами, разрушая как сами клетки, так и миелин. Болезнь развивается следующим образом.
- Разрушенные ткани постепенно заменяются прионом — чужеродным белком, играющим роль мощного антигена.
- На его появление и распространение иммунная система человека отвечает мощной аутоиммунной агрессией — происходит выработка антител.
- Последние направляются на уничтожение белого вещества нервных волокон, воспринимая его как чужеродный белок.
В результате иммунная система организма постепенно уничтожает нервную систему. В процессе развития патологии происходит поражение сразу нескольких ее отделов: оболочка постепенно разрушается и в ходе демиелинизации образуются очаги поражения — так называемые бляшки рассеянного склероза. Поскольку очаги поражения имеют рассеянный характер, склероз называется рассеянным. Само слово «склероз» в данном контексте означает «рубец» — это те самые спорадически распространяющиеся рубцы-бляшки (участки соединительной ткани), которые образуются на месте уничтоженных нервных тканей. Размер образований может доходить до нескольких сантиметров и более (если в ходе болезни они сливаются). Активные очаги, находящиеся в стадии образования, называют острыми.
Группы и факторы риска
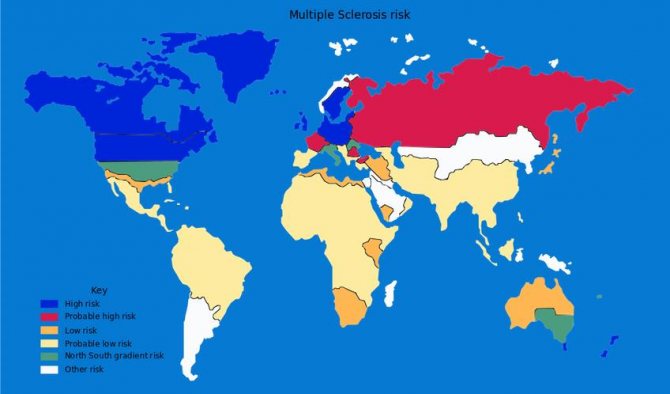
Темно-синим цветом выделены регионы с высоким риском заболевания РС, красным — с вероятно высоким риском.
Много ранее, задолго до появления технологии лечения рассеянного склероза стволовыми клетками, считалось, что основную группу риска составляют женщины в возрасте от 20 до 40 лет. Современный коллективный портрет больных весьма неоднороден: медики отмечают значительный рост случаев заболевания среди мужчин и женщин старше 40 лет. При этом у мужчин чаще всего протекает неблагоприятная прогрессирующая форма заболевания. Значительно чаще рассеянный склероз встречается сегодня среди европейцев — жителей северных регионов (Скандинавия, Северо-Запад России, Белоруссия). Таким образом, регион проживания сегодня признан одним из факторов риска, обусловливающих возможность появления рассеянного склероза. Помимо этого, в ряду других основных факторов:
- сосудистые заболевания;
- аутоиммунные заболевания;
- нарушенное психоэмоциональное состояние;
- инфекционно-аллергические заболевания;
- генетическая предрасположенность (изменение ферментных показателей, недостаточность Т-супрессоров).
Рассеянный склероз — клинические проявления
На фото: Бляшки — очаги демиелинизации
Клинические проявления РС — прямое следствие очаговых поражений отделов головного мозга.
Симптоматика рассеянного склероза сложна и разнообразна. В ряду наиболее частых характерных проявлений назовем следующие.
- Нарушения двигательной системы, связанные с поражением мозжечка, — у больного появляются пошатывания при ходьбе, возникает неловкость в движениях, нарушается координация, повышается мышечный тонус в руках. В отдельных случаях возникают парезы, случаются параличи.
- Нарушение зрения — возможно нарушение движения глазного яблока, появление «пелены» перед глазом или черной точки по центру поля зрения, при этом снижение зрения (вплоть до его потери) характерно для одного глаза.
- Нарушение функций тазовых органов — недержание мочи.
- Снижение вкусовой чувствительности.
- Поражение лицевого нерва с ослаблением мышц на одной стороне лица.
- Нарушения психической сферы — неврозоподобные состояния, астенический синдром, депрессия и т.д.
- Быстро наступающая усталость, утомляемость даже после незначительных физических и умственных нагрузок.
Рассеянный склероз
— весьма «коварное» заболевание: после появления первых проявлений симптоматика может исчезнуть на довольно длительный срок (даже на 10 — 15 лет), однако впоследствии, при отсутствии лечения болезни, она обязательно даст о себе знать в более тяжелых проявлениях. Кроме того, обострение болезни может быть спровоцировано перегреванием и переохлаждением, ОРВИ и другими заболеваниями, нервно-эмоциональными перегрузками.
Рассеянный склероз по степени тяжести
- Легкий тип: ремитирующее течение РС — обострения редки, периоды ремиссии — длительны.
- Среднее по тяжести течение — ремитирующе-прогрессирующее.
- Тяжелое, прогрессирующее течение (может быть первичным или вторичным).
Рассеянный склероз по форме
Форма рассеянного склероза определяется в зависимости от преобладающих симптомов. Выделяют спинальную, церебральную, глазную, гиперкинетическую, а также атипическую форму РС.
В Петербурге пациентов с рассеянным склерозом лечат с помощью стволовых клеток и химиотерапии
— Вы подчеркиваете, что прежде ТГСК проводилась на «жесткой» химиотерапии. Как ее проводят сегодня?
— Не проводится супервысокодозная химиотерапия, эффект при аутоиммунных болезнях достигается более низкими дозами. То есть, все равно с помощью химиопрепаратов мы «убиваем» аутоиммунные лимфоциты, подавляем причину развития заболевания — патологическую активность иммунитета, поддерживающую воспалительный процесс в мозге, из-за которого поражается миелин — защитная оболочка нейронов. Условно говоря, при ТГСК происходит то же самое, что и при приеме ПИТРС 2-й линии, просто доза лекарства намного выше. Но важно понимать, что зерно рассеянного склероза посеяно не в нервной системе, а по другую сторону гематоэнцефалического барьера, преодолеть который сложно. Но это как раз и дает нам возможность влиять на основную причину, запускающую агрессию по отношению к миелину, – то есть кровь и лимфатическую систему. Другими словами, мы не тушим костер, а перестаем подкладывать в него хворост — сокращаем количество аутоиммунных лимфоцитов и антител в крови.
Поэтому надо понимать, что не трансплантация оказывает основной лечебный эффект, а высокая доза иммуносупрессивного препарата. Поэтому, чтобы не пугать тех, кто застрял в 1990-х, лучше использовать понятие «высокодозная иммуносупрессивная терапия (ВИСТ) с последующей аутологичной трансплантацией гемопоэтических стволовых клеток — (ВИСТ+АТГСК)». Тем не менее, иммуносупрессия без трансплантации чревата тем, что в определенном проценте случаев костный мозг может не восстановиться, а это высокий риск смертельного исхода: любая иммуносупрессия приводит к тому, что в организме активируются «дремлющие» вирусы. Чтобы этого не произошло, после нее нужна трансплантация стволовых клеток, с помощью которой достигается более быстрое восстановление параметров крови в ответ на подавление иммунитета химиотерапией. Еще одна немаловажная роль непосредственно ТГСК – иммунная реконституция (в простонародье «перезапуск» иммунной системы): мы вводим человеку его собственные гемопоэтические стволовые клетки (CD34+), которые еще не перешли в стадию лимфоцитов.
— А какой смысл при аутоиммунных заболеваниях переливать свои клетки? Организм выработает такие же.
— Мы пока не можем доказать, что рассеянный склероз является генетически обусловленным заболеванием, хотя знаем о потенциальной иммуногенетической предрасположенности к этому заболеванию. Если бы рассматривался вопрос о применении ауто-ТГСК пациенту с «семейной» формой рассеянного склероза, то логики в аутотрансплантации, действительно, было бы меньше. Сейчас мы говорим о важности достижения так называемой иммунной «перезагрузки» с умеренными дозами химиотерапии и с переливанием собственных клеток пациента без серьезных осложнений, например, реакции «трансплантат против хозяина».
— Что должен делать пациент, который хотел бы сделать трансплантацию?
— Все-таки хотелось бы, чтобы мотивация на ее проведение исходила от лечащего врача. Если на всех предыдущих этапах лечения возможности исчерпаны и невролог выносит решение о проведении ТГСК по неврологическим показаниям, то готовность к лечению в гематологическом трансплантационном стационаре (и никак иначе) складывается из отсутствия активной воспалительной и тяжелой сопутствующей патологии.
— Что представляет собой процесс трансплантации? Звучит пугающе…
— После этапа подтверждения диагноза, анализа критериев «за» и «против», подготовки к ТГСК пациент госпитализируется в гематологическое отделение. Там в течение нескольких дней с помощью специальных препаратов стимулируется выход стволовых клеток (CD34+) из костного мозга в периферическую кровь, и они забираются с помощью аппарата для афереза (как при донации крови).
Пока полученные клетки готовятся к трансплантации, у пациента восстанавливается работа костного мозга. На следующем этапе проводится высокодозная иммуносупрессия (введение химиопрепарата), а затем переливание собственных, ранее заготовленных, клеток в вену пациента. Таким образом, это не хирургическая в классическом понимании, а сложная терапевтическая операция. Затем начинается этап восстановления параметров крови, которые изменяются в результате применения химиотерапии. Госпитализация длится в общей сложности не более 30 дней.
— Аутоиммунных заболеваний насчитывается достаточно много, это ведь не только рассеянный склероз, системная красная волчанка, склеродермия, ревматоидный артрит, васкулит, антифосфолипидный синдром и т. д. Предпринимаются ли попытки лечить их таким же способом?
— Действительно, описано уже около 100 аутоиммунных синдромов и болезней. Терапевтические подходы к ним схожи, и в «трансплантационном мире» они активно и эффективно используются. В нашем университете, например, недавно успешно выполнили такое лечение пациенту, страдающему одновременно склеродермией и красной волчанкой. Официально в регистре Европейского сообщества по трансплантации костного мозга (ЕВМТ), куда мы также подаем данные, зарегистрировано более 3000 трансплантаций при аутоиммунных заболеваниях. Более 1300 из них выполнены пациентам с рассеянным склерозом, около 800 – с заболеваниями соединительной ткани, более 220 – при воспалительных заболеваниях кишечника. Установлено, что риск этой процедуры при других тяжелых аутоиммунных заболеваниях выше, поскольку в отличие от рассеянного склероза, при них часто поражаются внутренние органы.
Справка
Первая ТГСК при аутоиммунных заболеваниях в нашей стране была выполнена в НИИ ФКИ в Новосибирске в 1998 году. У истоков ТГСК при рассеянном склерозе также стояли петербургские профессора Андрей Новик и Борис Афанасьев. Первая в России диссертация на эту тему была защищена в 2006 году в ПСПбГМУ им. Павлова. В Петербурге лечение пациентов с рассеянным склерозом изначально проводилось при взаимодействии с неврологами на базе НИИ Детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой, как члена Европейского общества по трансплантации крови и костного мозга (EBMT).
Лечение рассеянного склероза
Этиотропная терапия РС, т.е. лечение, направленное на устранение конкретной причины заболевания, не практикуется в силу невозможности выявить его конкретный возбудитель. Вследствие этого применяется патогенетическая терапия, главными задачами которой являются:
- купирование обострения заболевания с воздействием на очаги аутоиммунного воспаления и одновременной активизацией компенсаторно-приспособительных механизмов;
- предотвращение и уменьшение выраженности обострений;
- симптоматическая терапия по устранению симптомов, негативно сказывающихся на возможности пациента вести привычный образ жизни.
В ходе лечения рассеянного склероза используются плазмаферез, глюкокортикоиды, копаксон, адренокортикотропный гормон, биостимуляторы, витамины группы В и другие препараты.
Этапы лечения с помощью трансплантации стволовых клеток
Шаг первый – Подготовка стволовых клеток. В первую очередь, донор предоставляет врачам полную историю своей болезни. Кроме того, у пациента берут анализы, такие как химия крови, серология для инфекций, определяется группа крови, резус-фактор, делается кардиограмма, визуализация и спирография. Также обязательна поясничная пункция и МРТ с контрастом и без него. Затем из периферической крови извлекают гемопоэтические стволовые клетки посредством подкожных инъекций. Этого может быть достаточно для трансплантации стволовых клеток больному рассеянным склерозом.
Если же этот метод оказывается не эффективным, в этом случае стволовые клетки собирают из костного мозга тазовой кости (подвздошный гребень). Это не сложная операция, которую делают под местной анестезией, реже — общим наркозом.
Шаг второй – Трансплантация стволовых клеток при рассеянном склерозе. Перед тем, как пересадить здоровые клетки, больной рассеянным склерозом проходит так называемую процедуру кондиционирования, которая подавляет иммунную систему, чтобы она не отторгла новые стволовые клетки. По сути, это химиотерапия. Безусловно, это риск, поскольку иммунитет фактически разрушается, человек становится очень чувствительным к любым инфекциям, даже легкая простуда может привести к летальному исходу. Поэтому пациент находится в стационаре, в специальной стерильной палате. Но период при лечении рассеянного склероза недолгий – всего неделя.
После чего, происходит непосредственно трансплантация. Здоровые клетки, посредством инъекций вводятся больному. Дальше самое сложное – ожидание. Состояние рецепиента ежедневно контролируется: регулярно берут кровь для анализов, проверяют как растут новые стволовые клетки и восстанавливается иммунитет. Чаще всего, на то, чтобы результаты анализов пришли в норму, уходит от 10 до 14 дней. Когда это происходит – пациента выписывают.
Шаг третий – Лечение рассеянного склероза и укрепление иммунитета. После выписки, пациент обязательно проходит курс лечения, направленный на укрепление иммунитета, а также на профилактику воспалительных процессов. Один раз в три-четыре дня необходимо посещать врача и сдавать анализ крови, для контроля за общим состоянием больного. Средняя длительность такого лечения – до двух месяцев. По прошествии этого времени и в зависимости от результатов анализов, врач назначает даты контрольных исследований по поводу рассеянного склероза.
Сделайте заявку на лечение
Нажимая эту кнопку, вы получаете быстрый отклик и индивидуальное решение от врача
Лечение РС стволовыми клетками в нашей клинике
Один из наиболее эффективных методов борьбы с коварным недугом — лечение рассеянного склероза стволовыми клетками. Именно этот прогрессивный и действенный метод заместительной терапии сегодня предлагается в передовых клиниках Санкт-Петербурга. Он обеспечивает:
- восстановление миелина, а вместе с ним — и нормальной скорости передачи нервных импульсов;
- регенерацию клеток головного и спинного мозга на участках нервных тканей, замещенных соединительной рубцовой тканью;
- нормализацию деятельности иммунной системы с прекращением аутоиммунных «атак» с ее стороны на нервную систему организма.
На раннем этапе развития болезни возможно излечение РС благодаря мощному регенеративному потенциалу стволовых клеток. Метод лечения рассеянного склероза стволовыми клетками характеризуется достижением высоких результатов: в каждом из имевших место случаев терапевтического воздействия он обеспечивает стойкую ремиссию. В результате проводимых терапевтических процедур пациенты клиники вновь обретают моторику двигательных функций, возможность полностью обслуживать себя, самостоятельно передвигаться, иными словами — возможность жить полноценной жизнью.
Трансплантация гемопоэтических стволовых клеток в лечении рассеянного склероза
Гемопоэтические стволовые клетки признаны в качестве СК более 40 лет назад. В последние годы доказана высокая пластичность ГСК, которые могут быть источником происхождения не только клеток крови, но и специфических клеток других тканей – мышц, кровеносных сосудов, клеток печени и нервной системы и др. ГСК отличаются четырьмя свойствами: способны к самовоспроизведению; дифференцируются в специфические клетки; могут быть мобилизованы из костного мозга и обратно; для них характерна программируемая гибель (апоптоз).
К числу первых заболеваний, при которых вполне естественно стали использовать с лечебной целью ГСК, относятся гемобластозы (острые лейкозы, миеломная болезнь, лимфогрануломатоз и пр.). При перечисленных заболеваниях опухолевые гемопоэтические клетки разрушаются с помощью больших доз химиотерапии и/или общего облучения с последующим восстановлением нормального гемопоэза путем трансплантации аллогенных ГСК от доноров, совместимых с реципиентом по лейкоцитарным антигенам (HLA).
К середине 90-х годов прошлого столетия число трансплантаций гематогенных (гемопоэтических) стволовых клеток в 12 ведущих странах Европы достигло 16-17 операций на 1 млн. человек, большинство из которых проведено при лейкемии, анемии, наследственных дефектах метаболизма. По аналогии с лечением гемобластозов изучают возможность использования ГСК с целью «реконструирования» «репрограмирования» иммунной системы при некоторых аутоиммунных заболеваниях – системной красной волчанке, ревматоидном артрите, сахарном диабете типа 1. При перечисленных заболеваниях больным вводили большие дозы цитостатиков или проводили общее облучение, что вызывало гипоплазию или аплазию гемопоэза и клеток иммунной системы, с последующим введением собственных (аутологичных) или донорских (аллогенных) ГСК, вызывающих восстановление кроветворения и иммунной системы.
Рассеянный склероз (РС) как хроническое мультифакториальное аутоиммунное заболевание ЦНС, характеризующееся непрерывным течением во времени и проявляющееся либо в виде отдельных обострений, либо в форме непрерывно прогрессирующего процесса, закономерно становится объектом внимания исследователей, занимающихся СК.
Применяемые в настоящее время методы лечения РС малоэффективны. Это явилось причиной поиска новых более эффективных способов терапии. Одним из наиболее перспективных методов лечения РС, эффективность которого в настоящее время изучается во многих медицинских центрах, является трансплантация гемопоэтических стволовых клеток (ТГСК).Применение ТГСК позволило сделать прорыв в лечении многих онкологических и гематологических заболеваний. В настоящее время изучается эффективность данного метода лечения у больных с аутоиммунными заболеваниями, в том числе больных РС.
Высокодозная иммуносупрессивная терапия (ВДТ) в сочетании с трансплантацией стволовых кроветворных (гемопоэтических) клеток (ТГСК) – принципиально новый подход, предполагающий возможность излечения ряда форм РС. Главная задача ВДТ + ТСКК при аутоиммунных заболеваниях, в том числе при РС, – эрадикация пула аутореактивных лимфоцитов и их предшественников. Проведенные клинические исследования в рамках EBMT (европейской группы по трансплантации костного мозга, European Bone Marrow Transplantation Group) показали, что данный метод лечения у 79,3%больных приводит к улучшению состояния. Однако, с целью получения более выраженного эффекта в настоящее время изучаются подходы с предварительной элиминацией иммунокомпетентных клеток методами in vitro или in vivo. Одним из таких подходов является применение антитимоцитарного иммуноглобулина как одного из компонента ТГСК, а также применение препаратов снижающих количество иммунокомпетентных клеток перед забором ГСК. В настоящее время имеются немногочисленные данные о применении кладрибина перед забором ГСК, что позволяет значительно уменьшить содержание иммунокомпетентных клеток в трансплантате. В нашей стране недавно закончены клинические испытания отечественного аналога кладрибина — препарата «лейкладин»при ряде онкогематологических заболеваний и при рассеянном склерозе.
Перспективы
Несмотря на существенный прогресс, достигнутый в изучении СК, для их широкого клинического применения необходимо решить много важных практических вопросов. Например, как долго могут функционировать трансплантированные клетки; отражают ли результаты исследований, выполненных на лабораторных животных, ситуацию с возможностью применения СК у человека; соответствует ли нейротрансмиттерная нейрональная сеть замещенных нейроглиальных комплексов нативным нейронам и глии? И, тем не менее, уже сейчас можно констатировать, что как в неврологии, так и в нейрохирургии лечебные технологии с использованием СК будут и дальше развиваться и, по-видимому, со временем смогут занять достойное место в ряду методов коррекции нарушений деятельности нервной системы. В частности, создаются специальные генно-модифицировнные линии нейронов и глии с целью пересадок и заместительной терапии. Эти клетки имеют высокую инвазивность, пролиферативную активность для создания ростков здоровой ткани и не опасны в плане канцерогенеза. Проводится интенсивное изучение генов, сигнальных молекул и ростовых факторов, контролирующих активное размножение и выживание донорских клеток в нервной ткани.
Долгое время считалось, что острые травматические повреждения ЦНС необратимы из-за отсутствия пролиферации нейронов в зоне поражения и невозможности повторного роста аксона у нейронов. Причину искали в свойствах окружающей астроглии, блокирующей регенерацию нервных клеток. Однако последние эффективные пересадки иммортализованных клеток в поврежденный спинной мозг доказывают возможность восстановления нервных связей мотонейронов, если имплантант размещали дистальнее повреждения. Столь же эффективными оказались пересадки нейробластов в разные зоны механически поврежденного головного мозга.
К числу неврологических заболеваний, при которых предполагается возможность применения с лечебной целью СК, относится
- паркинсонизм,
- хорея Гентингтона,
- боковой амиотрофический склероз,
- инсульт,
- ранние формы болезни Альцгеймера,
- травматические поражения нервной системы,
- рассеянный склероз.
Паркинсонизм считают одним из первых заболеваний, при котором можно будет использовать трансплантацию СК с лечебной целью и ожидать реальных результатов.
Исследователи из Университета Джона Гопкинса использовали человеческие зародышевые СК для восстановления двигательных нейронов у крыс с моделью бокового амиотрофического склероза, индуцированного нейротропным вирусом. Выжившим после заражения животным с параличом конечностей вводили СК в ткани, смежные с разрушенными моторными нейронами спинного мозга. G.Steinberg, e.a. из отдела нейрохирургии Стендфордского университета у крыс с моделью инсульта изучали выживаемость, миграцию, дифференцировку и функциональные свойства человеческих зародышевых нервных СК. Через 5 нед. после введения СК наблюдали их миграцию в область повреждения и дифференцировку в нейроны. Результаты этого исследования свидетельствуют о потенциальной возможности использования СК в лечении мозгового инсульта. Особенности биологии мышечных СК, которые состоят в том, что они в отличие от других ВСК при введении реципиентам не отторгаются их иммунной системой, поскольку на поверхности этого вида СК отсутствуют белковые маркеры, позволяют рассчитывать на возможность их использования при лечении некурабельного генетического заболевания – миодистрофии Дюшенна. Так, введение в дистрофичные мышцы мышечных СК mdx-мышам с моделью данного заболевания приводило к «реконструированию» 25% мышечных клеток.
Результаты изучения свойств ЭСК и ВСК свидетельствуют об огромных потенциальных возможностях их использования в лечебной практике. Во многих исследованиях показано, что и ВСК, и ЭСК могут восстанавливать поврежденные органы и ткани. В плане практического применения СК остается еще много нерешенных вопросов. Можно ли будет, в частности при РС, ограничится только лишь ВСК? Сколько разных источников СК потребуется в короткие сроки для получения нужного их количества? Пока невозможно предсказать какие СК – ЭСК, зародышевые или ВСК будут в наибольшей степени соответствовать клиническим задачам. Для ответа на эти вопросы необходимо проведение большого количества исследований.
В заключение следует сказать, что создание в перспективе национального банка СК (ЭСК, ГСК, ВСК), например, на базе Республиканского центра трансплантации костного мозга, позволило бы интегрировать и унифицировать научно-практическую деятельность в республике, направленную на использование клеточных технологий не только в онкогематологии но и в неврологии и нейрохирургии и других областях практической медицины.
Процедура лечения РС стволовыми клетками
Та или иная методика терапии выбирается в зависимости от формы течения РС и тяжести протекания заболевания. Процедура лечения РС стволовыми клетками осуществляется в несколько этапов.
- На первом выполняются медикаментозные процедуры с использованием уже упомянутых плазмафереза, копаксона и других препаратов — в зависимости от формы рассеянного склероза, специфики протекания заболевания и других факторов. Основная задача на первом этапе процедур — приостановление процесса разрушения миелина и купирование иммуновоспалительного процесса.
- На втором, третьем, а при необходимости и на четвертом этапе лечения рассеянного склероза осуществляется трансплантация стволовых клеток. Это собственные мезенхимальные стволовые клетки, выделенные из биоматериалов пациента — костного мозга и жировой ткани.
Процедуры трансплантации осуществляются с месячным интервалом. Как правило, в ходе одной процедуры в кровь пациента вводятся клетки в количестве из расчета 1 млн на 1 кг тела пациента (например, для пациента с массой тела 70 кг необходимо введение 70 млн клеток). Уже в течение короткого времени организм больного демонстрирует первые признаки улучшения, связанные с нормализацией приема и передачи нервных импульсов и восстановления популяции нейронов.
- Через 1,5-2 месяца улучшается ситуация с удержанием равновесия, происходит восстановление чувствительности, улучшается психологическое состояние.
- В течение 3-4 месяцев нормализуется походка, восстанавливается память, исчезает двоение в глазах.
- В течение года прекращается образование новых зон демиелинизации и появление новых рубцов.
Наступает стойкая ремиссия. Исчезает неврологическое расстройство, восстанавливается память, преодолеваются симптомы хронической усталости. Полностью восстанавливается работа речевого аппарата. Достигнутый терапевтический эффект может длиться годами, в зависимости от образа жизни пациента (отсутствие вредных привычек и т.д.). Человек обретает возможность полноценной жизни в социуме.
Эффективность стволовых клеток при рассеянном склерозе
Рассеянным склерозом именуется особая патология нервной системы — когда-то ее считали неизлечимой, сегодня же специалисты способны справиться с этим недугом при условии своевременно начатого лечения. Полноценный шанс на выздоровление предоставляет операция по пересадке стволовых клеток — такая методика считается инновационной, однако до сих пор признана не во всех странах.
Как показывает практика, пересадка стволовых клеток успела зарекомендовать себя с лучших сторон. После подобного вмешательства качество жизни пациентов существенно повышается.
Откуда берётся рассеянный склероз
Для того чтобы понять, какая схема терапии будет оптимальной для лечения рассеянного склероза, необходимо выяснить первопричину данного заболевания в каждом конкретном случае. По сей день специалисты не могут достоверно сказать, почему болезнь проявляется у того или иного человека. В числе провоцирующих факторов перечисляются:
- генетическая предрасположенность — у ребенка вполне возможно проявится такое заболевание, если ранее у его родственников наблюдались признаки рассеянного склероза;
- излишние интеллектуальные нагрузки, которые провоцируют психологическую нестабильность и стресс, что тоже может привести к заболеванию;
- ослабление иммунной системы, сопровождающееся частыми инфекциями и поражением структур головного мозга;
- аутоиммунные заболевания – они также могут выступать в качестве провоцирующих факторов, когда организм перестает воспринимать свои же ткани, считая их чужеродными и создавая защитные клетки, что вызывает хроническое течение воспаления и подрыв деятельности нервной системы;
- вредные привычки увеличивают риск возникновения рассеянного склероза, если человек злоупотребляет алкоголем и табаком несколько десятков лет, то шансы на то, что он столкнется с данным заболеванием, резко увеличиваются.
Как определить наличие рассеянного склероза
Лечение болезни невозможно без определения её проявлений. Последние напрямую связаны с поражением нервных волокон, а потому клиническая картина полностью зависит от той части тела, в которой сформирован очаг заболевания. К числу основных проявлений рассеянного склероза можно отнести:
- тремор конечностей;
- нарушение восприятия тела в пространстве;
- нарушение координации движений;
- отсутствие контроля над мышцами лица;
- покалывание кожных покровов;
- нетипичные проявления мышечного тонуса;
- сбои в мочеиспускании в сторону недержания.
Неврологически перечисленные симптомы проявляются, как смена настроения пациента, которое может варьироваться от плаксивости и депрессии до эйфории. Перед тем, как определить, действительно ли конкретному больному поможет пересадка стволовых клеток, специалист должен провести неврологический осмотр и исследовать нервную систему инструментально.
Что представляет собой методика пересадки стволовых клеток
Данный процесс основан на способности стволовых клеток дифференцироваться в конкретные зоны человеческого организма. В нашей стране трансплантация их при рассеянном склерозе допустима на законодательном уровне. Доказано, что подобная терапия приводит к полному восстановлению миелиновой оболочки волокон нервов мозга, положительно отражается она и на состоянии иммунной системы.
Важно! Использование стволовых клеток для лечения рассеянного склероза допустимо в случае, когда ранее уже применялись другие терапевтические мероприятия и значимого результата они не принесли. В обязательном порядке биоматериал необходимо забирать непосредственно от пациента, что позволяет снизить вероятность занесения инфекции, иммунологических несовпадений и возможных мутаций клеток.
Как проводится трансплантация
Данный процесс делится на три этапа, предварительно специалисты всегда оценивают исходное состояние здоровья человека, а также определяют ту стадию, в которой находится заболевание на конкретный момент времени.
Первым этапом является забор стволовых клеток. Учитывая, что дифференцировать нужные клетки в должном объеме сразу не представляется возможным, процедуру забора крови порой приходится проводить 3-4 раза. После этого полученные клетки замораживаются до пересадки.
Второй этап подразумевает уничтожение тех иммунных клеток, которые ранее были поражены патологическими процессами. Для этой цели применяют противовоспалительные и иммуносупрессивные препараты. Именно такое комплексное воздействие подготавливает организм к трансплантации.
Завершающим этапом является подача внутривенно в кровяное русло стволовых клеток.
От чего зависит результат лечения
Для того чтобы получить должный эффект и значительно повысить качество жизни пациента, необходимо соблюсти целый перечень условий. Повышенная эффективность процедур достигается, если воздействовать на заболевание в определённой стадии, контролируя его прогрессирование. Многое зависит от возраста больного и восприимчивости его тканей к такой терапии. Сопутствующие тяжёлые заболевания тоже имеют значение.
Больше всего шансов на выздоровление имеют пациенты на начальной стадии рассеянного склероза, так как в этом случае миелиновая оболочка регенерируется гораздо быстрее. Превосходный результат на практике демонстрировали и те люди, у которых рассеянный склероз наблюдался на протяжении 7-8 лет. После проведения нескольких процедур восстанавливалось большинство клеток, включая те, что были поражены на 80%.
Вероятные риски
Когда в организм пациента вводятся его собственные стволовые клетки, риск отторжения сводится к минимуму. В качестве исключения можно привести пример тех пациентов, которые изначально имели аутоиммунные патологии. В подобных ситуациях должный эффект можно получить посредством дополнительного приема медикаментов иммуносупрессивного типа. К числу осложнений после пересадки относятся редкие случаи:
- неправильно подобранного объёма материала;
- несоблюдения стерильности;
- недостаточной подготовленности организма;
- невыдержанного интервала между этапами введения стволовых клеток.
Важно! Крайне нежелательно вводить пациенту стволовые клетки другого человека — такое рискованное мероприятие может привести к летальному исходу.
Только ранняя диагностика заболевания и своевременное введение стволовых клеток с использованием специализированного оборудования и привлечением врачей высокой квалификации позволяет обеспечить полное выздоровление.